R. Vivanco Hidalgo
- Estimulador del nervio vago (ENV)
- Estimulación cerebral profunda
- Algoritmo de tratamiento
- Dieta cetogénica
- Bibliografía
Existe un grupo de pacientes con epilepsias graves que no responden al tratamiento farmacológico y no son candidatos quirúrgicos. En este subgrupo de pacientes existen otras alternativas que pueden mejorar su epilepsia. Los dispositivos y dietas que se van a comentar a continuación tienen un objetivo inicial paliativo, es decir, el objetivo del tratamiento/dispositivo es el de reducir la severidad y/o frecuencia de las crisis. No obstante, en un porcentaje variable de pacientes se llegará a un control completo de su epilepsia.
Estimulador del nervio vago (ENV)
Introducción
El ENV es un dispositivo de estimulación cerebral inicialmente aprobado por la FDA en el año 1997 para el tratamiento de la epilepsia focal farmacorresistente(1,2). Se trata de un dispositivo de estimulación abierto. Los parámetros de estimulación se programan de forma individual en cada paciente de tal forma que el estimulador manda estímulos eléctricos periódicos con las características que definamos. El mecanismo de acción no es del todo conocido: a través de sus fibras aferentes que llegan al núcleo del tracto solitario neuromodula diferentes estructuras centroencefálicas y corticales. El dispositivo consta de un generador que se implanta subcutáneamente a nivel infraclavicular desde donde manda pulsos eléctricos intermitentes, a través de un electrodo que envuelve parcialmente el nervio vago izquierdo en la región cervical.
Parámetros de estimulación habituales
Los parámetros de estimulación se diseñarán de forma individual para cada paciente. Los parámetros más importantes que determinan la mejor respuesta clínica y, de forma paralela, los responsables de los posibles efectos adversos son la corriente de salida, la frecuencia de señal y el tiempo encendido. El ENV dispone de un imán que al pasarlo sobre el generador en el pecho pondrá en marcha unos parámetros de estimulación superiores a los basales (generalmente, se programa para que la corriente de salida sea 0,25 mA superior que la basal). El objetivo de esta estimulación "extra" a través del imán es el de abortar las crisis focales en las que el paciente identifica un aura; será el propio paciente o un familiar/testigo el que pase el imán sobre el pecho cuando el paciente perciba que va a tener una crisis (Tabla I).
Tabla I. Parámetros de estimulación.
|
Parámetros |
Rango |
Parámetros habituales |
|
Corriente de salida (mA) |
0-3,5 |
1-2 En niños suele ser superior |
|
Frecuencia de señal (Hz) |
1-30 |
20-30 |
|
Ancho de pulso (µs) |
130-1.000 |
250-500 |
|
Tiempo ON (s) |
7-60 |
30 |
|
Tiempo OFF (min) |
0,2-180 |
5 |
Indicaciones
- • Epilepsia focal refractaria sin posibilidad de cirugía (>12 años), tanto en pacientes con CPC como SGTC.
- • Epilepsia focal con cirugía fallida.
- • Otros síndromes epilépticos (en base a diferentes estudios se describen resultados positivos en epilepsias pediátricas como síndrome de Lennox-Gastaut, esclerosis tuberosa, epilepsias generalizadas sintomáticas, etc.).
- • Está contraindicado en pacientes con vagotomía izquierda y alteraciones severas de la conducción cardiaca.
- • Se pueden realizar RMN (1,5 y 3T) si se ajustan el tipo de bobinas adecuadas. Además, la corriente de salida del generador del ENV se debe poner a 0 mA.
Eficacia clínica/efectos adversos
Los estudios clínicos publicados muestran resultados variables. De forma general:
- • Reducción media de crisis de alrededor del 30% en los 3 primeros meses(1).
- • Efecto acumulativo ("a largo plazo") con disminución de crisis significativa (>50%) en aproximadamente un 35-50% de los pacientes implantados al cabo del año.
- • Libre de crisis <10%.
- • Posible mejoría del estado del ánimo, no efectos cognitivos.
- • Disminución de las caídas producidas por las crisis.
- • Los efectos adversos son infrecuentes y reversibles, ocurren típicamente durante la estimulación y disminuyen a lo largo del tiempo, se pueden disminuir al cambiar los parámetros y rara vez persisten tras suspender la estimulación. Los más frecuentes son: ronquera/alteración en la voz (19,3%), tos (5,9%), sensación disneica (3,2%).
Estimulación cerebral profunda
El número de núcleos cerebrales como dianas potenciales para estimulación cerebral ha aumentado en los últimos años; se han explorado dianas como el hipocampo, el núcleo subtalámico, el núcleo caudado, y los núcleos centromediano y anterior del tálamo. En la actualidad, existen dos dispositivos aprobados para uso clínico.
Estimulación del núcleo anterior del tálamo (NAT)
Introducción
El NAT es una diana muy atractiva para la estimulación cerebral, debido a la existencia de numerosas proyecciones tálamo-corticales con regiones frontales y temporales que forman parte del circuito de Papez. La estimulación del NAT en modelos animales produce sincronización/desincronización cortical en función de las frecuencias del estímulo eléctrico aplicado. Además, dentro de los núcleos profundos cerebrales, el NAT tiene un tamaño y localización que lo hace más accesible que otros centros. Al igual que el ENV, el dispositivo empleado para la estimulación del NAT es un dispositivo abierto que estimula de acuerdo a unos parámetros establecidos. Este sistema requiere de la implantación de dos electrodos profundos por cirugía esterotáxica en ambos NAT.
Indicaciones
- • Pacientes adultos con epilepsia focal farmacorresistente grave, no candidatos quirúrgicos o con cirugía fallida.
- • La implantación previa de un ENV no contraindica la implantación de este dispositivo.
Eficacia clínica/efectos adversos
Los resultados de eficacia y seguridad de este dispositivo se basan en el estudio SANTE (Stimulation of the Anterior Nucleus of Thalamus for Epilepsy), recientemente publicado(3):
- • Reducción de crisis >50%: 54% de los pacientes a los dos años.
- • Reducción media de crisis del 40,4% a los tres meses (fase doble ciego del ensayo) y del 56% a los dos años de la implantación.
- • Un 13% de pacientes llegan a estar 6 meses sin crisis.
- • Tal vez mejor resultados en epilepsias temporales.
- • Reacciones adversas más significativas: depresión en 14% de pacientes, alteración de memoria en el 13% de pacientes.
Estimulación cerebral de circuito cerrado (RNS)
Introducción
El RNS (Responsive Neurostimulation, NeuroPace) es un dispositivo implantable diseñado para el tratamiento de la epilepsia focal refractaria. El NeuroPace, a diferencia de los otros dispositivos comentados, es un estimulador de circuito cerrado, programado para identificar los posibles patrones ictales de cada paciente de forma individual y abortarlas mediante un estímulo eléctrico antes de que el paciente experimente los síntomas de la crisis. Se implanta en el cráneo y es capaz de estimular distintas estructuras cerebrales mediante electrodos profundos y/o subdurales.
Indicaciones
- • Pacientes adultos con epilepsia focal grave farmacorresistente.
- • La zona epileptógena que genera las crisis ha sido correctamente identificada.
- • Potencialmente más útil en pacientes con epilepsias multifocales (varias regiones cerebrales que generan crisis) o con lesiones sobre zonas cerebrales elocuentes y, por lo tanto, no resecables.
Eficacia clínica/efectos adversos
Los resultados de eficacia de este dispositivo se basan en un estudio recientemente publicado (RN System Pivotal Trial)(4).
- • Reducción de crisis >50%: 43% de los pacientes al año, 46% a los dos años.
- • Reducción media de crisis del 38% durante la fase doble-ciega (solo del 17% en el grupo no estimulado).
- • 7% libres de crisis.
- • Alrededor de un 5% de los pacientes empeoraron (mayor número de CGTC y CPS).
- • Reacciones adversas más significativas: infecciones graves 4,2%, hemorragia severa 2,1%, cefalea en el 10%.
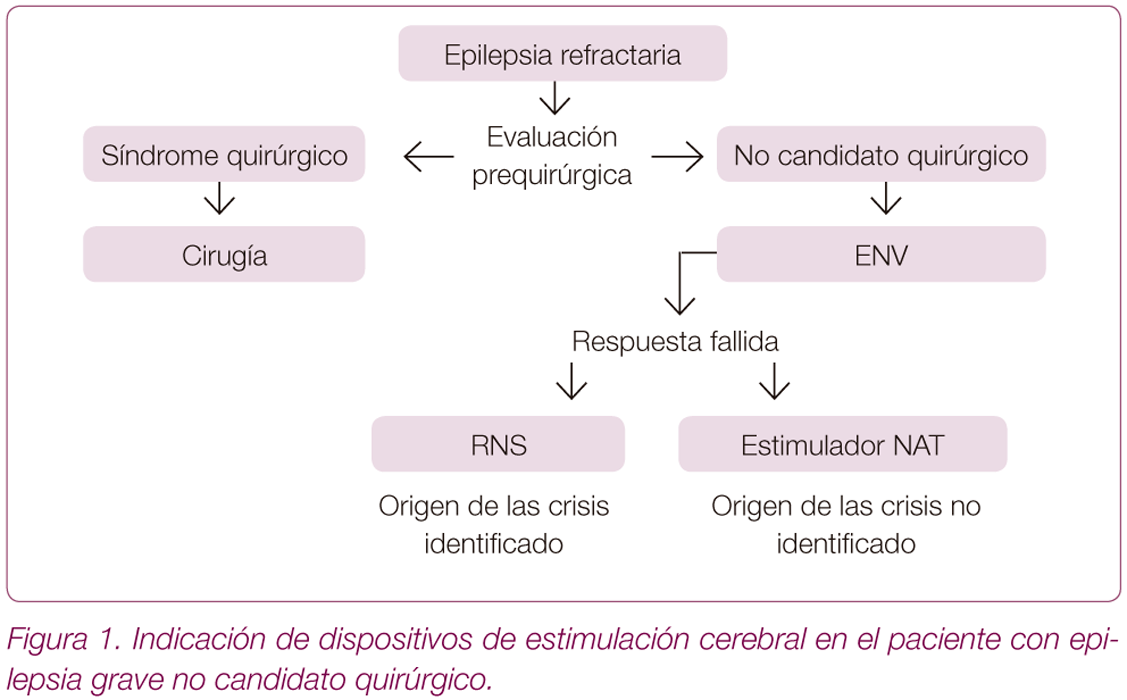
Algoritmo de tratamiento (Figura 1)
En todo paciente con epilepsia grave no controlada con fármacos antiepilépticos se debe realizar una evaluación prequirúrgica. Aunque las indicaciones de los nuevos dispositivos no están claramente establecidas, en base a las características de los mismos y de los resultados de los estudios pivotales se puede plantear este posible algoritmo.
Dieta cetogénica
Introducción
Dieta específica para el tratamiento de la epilepsia en la que el aporte calórico se realiza fundamentalmente a través de grasas, restringiéndose el consumo de proteínas e hidratos de carbono. Este tipo de dieta remeda los cambios metabólicos y de uso energético que se ponen en marcha durante el ayuno: al limitarse el aporte de hidratos de carbono y azúcares el cerebro obtiene la energía necesaria a través del metabolismo de las grasas, generándose cuerpos cetónicos que se convierten en el sustrato energético cerebral. El mecanismo de acción a través del cual este tipo de dieta mejora el control de las crisis es controvertido. Se piensa que los propios cuerpos cetónicos pueden ser antiepilépticos. Otras teorías consideran otros metabolitos o cambios en la homeostasis como responsables de la eficacia de este tratamiento (p. ej. a través del cambio del PH cerebral, aumento de los aminoácidos aromáticos plasmáticos, aumento de los ácidos grasos poliinsaturados, aumento del GABA, o modulación de la glicolisis cerebral entre otros).
Indicaciones
- • Epilepsias refractarias graves, focales y generalizadas (encefalopatías).
- • Eficaz en el tratamiento de distintos tipos de crisis.
- • Déficit del GLUT-1 (tratamiento específico +/- FAE).
- • Déficit de la piruvato deshidrogenasa (tratamiento específico +/- FAE).
- • Aunque es más fácil de implementar en la edad pediátrica también se puede emplear en adultos.
Contraindicaciones
- • Déficit de carnitina.
- • Déficit de la carnitina palmitoil transferasa tipo I y II.
- • Déficit carnitina translocasa.
- • Déficit de piruvato carboxilasa.
- • Porfiria.
- • Precaución si existen antecedentes de nefrolitiasis.
Tipos de dietas
En función de la proporción entre grasas y proteínas/hidratos de carbono existen distintos tipos de dietas.
Dieta cetogénica clásica (DCC)
La DCC se basa en un alto contenido graso, con una proporción de 4:1 o 3:1 de grasas respecto a proteínas y carbohidratos. La dieta 3:1 suele emplearse inicialmente en niños más pequeños al ser mejor tolerada por permitir más hidratos de carbono y más proteínas. La duración de la dieta es variable en función de cada paciente (respuesta clínica y posibles efectos adversos). En general, es necesario mantenerla alrededor de 2-3 meses para poder sacar conclusiones sobre su eficacia. En los pacientes con respuesta clínica favorable se suele mantener alrededor de 1-2 años, existiendo periodos de "descanso" donde se evalúa al paciente sin la misma. En muchos centros se ingresa al paciente para el inicio de la DDC con dos objetivos:
- • Vigilar la posible aparición de hipoglucemias durante el ayuno, especialmente en niños pequeños.
- • Instruir a la familia y al paciente sobre los alimentos de la DDC y la forma en la que se debe realizar.
Dieta cetogénica de triglicéridos de cadena media (MCT)
En la dieta MCT se utilizan triglicéridos de cadena media, ácidos grasos que son mejor tolerados que los de cadena larga empleados habitualmente en la DCC. De igual forma, los triglicéridos de cadena media son más cetogénicos, lo que permite emplear una proporción más levada de proteínas y carbohidratos. La eficacia de esta dieta es similar a la DCC.
Dieta modificada de Atkins (MAD)
Es una dieta menos estricta que las anteriores y, por lo tanto, más fácil de seguir. Se basa en una alimentación con alto contenido en ácidos grasos con restricción parcial de hidratos de carbono (10 g/día). No existe limitación en el consumo de proteínas. La aparición de cuerpos cetónicos es variable.
Dieta con bajo índice glucémico (LGIT)
Permite 40-60g/d de CH de bajo índice glucémico (<50). El índice glucémico es una medida de cuánto elevará la concentración de glucosa una determinada comida comparada con una cantidad de glucosa equivalente. Es una dieta menos restrictiva que la DDC y que permite administrar hidratos de carbono (40-60 g/día) con bajo índice glucémico.
Comparación entre dietas
La elección de cada tipo de dieta debe hacerse de forma individual, considerando la edad del niño, circunstancias familiares, disponibilidad del dietista y del seguimiento que se va a realizar. En los niños menores de 2 años, o sometidos a nutrición enteral se suele emplear inicialmente la DCC. En niños más mayores se pueden emplear otras dietas. También puede considerarse cambiar de una dieta a otra después de cierto tiempo según la evolución clínica y la tolerancia a la misma (Tablas II y III).
Tabla II. Comparación de la dieta regular con las dietas cetogénicas.
|
|
Regular |
LGIT |
MAD |
MCT |
KD |
|
Grasas Proteínas Carbohidratos Proporción |
30% 20% 50% 0,2-0,3:1 |
60% 20-30% 10% 1:1 |
60-70% 20-30% 6% 1:1 |
30-60% 10% 15-19% N/A |
90% 6-8% 2-4% 3-4:1 |
Tabla modificada de Miranda MJ. Epilepsy Res 2012(5).
LGIT: Bajo índice glucémico. MAD: Modificada de Atkins. MCT: Triglicéridos de cadena media. KD: Dieta cetogénica.
Tabla III. Comparación de dietas cetogénicas "clásicas" y "alternativas".
|
Dietas cetogénicas
|
Dietas cetogénicas "alternativas"
|
|
Restricción de HC < 10 g/d (> en MCT) Cetosis mantenida Restricción calórica leve/moderada Comidas calculadas por el dietista |
Restricción de HC > 10 g/d Grado de cetosis variable (incluso ausente) Sin restricción calórica o proteica Comidas recomendadas por el dietista |
Tabla modificada de Miranda MJ. Epilepsy Res 2012(5).
DCC: dieta cetogénica clásica . LCT: Dieta cetogéncia de triglicéridos de cadena larga. MCT-DC: Dieta cetogénica con triglicéridoss de cadena media.
Eficacia clínica/efectos adversos
Los resultados de eficacia proporcionados por los diferentes estudios no son del todo comparables debido a que la mayoría de los estudios son retrospectivos, han empleado una metodología diferente y se han realizado sobre poblaciones diferentes. Con relación a un ensayo clínico aleatorizado/controlado(6) se estima:
- • Tasa de respondedores (reducción del número de crisis >50%) del 38% a los tres meses.
- • Reducción de crisis >90% en el 7%.
- • No diferencia de eficacia entre DCC y MCT.
- • El porcentaje de pacientes libres de crisis a largo plazo es variable, según los estudios (7-25% a los 12 meses)(7).
- • Reacciones adversas más significativas: estreñimiento, náuseas y vómitos al inicio de la dieta, litiasis renal (5%, evitar fármacos como topiramato y zonisamida), déficit vitamínico (complementar con vitaminas), alteración del perfil lipídico, posible mayor riesgo de ateromatosis a largo plazo (controvertido).
Bibliografía
1. Handforth A, DeGiorgio CM, Schachter SC, Uthman BM, Naritoku DK, Tecoma ES, et al. Vagus nerve stimulation therapy for partial-onset seizures: a randomized active-control trial. Neurology. 1998;51:48-55.
2. Ben-Menachem E, Mañon-Espaillat R, Ristanovic R, Wilder BJ, Stefan H, Mirza W, et al. Vagus nerve stimulation for treatment of partial seizures: 1. A controlled study of effect on seizures. First International Vagus Nerve Stimulation Study Group. Epilepsia. 1994;35:616-26.
3. Fisher R, Salanova V, Witt T, Worth R, Henry T, Gross R, et al; SANTE Study Group. Electrical stimulation of the anterior nucleus of thalamus for treatment of refractory epilepsy. Epilepsia. 2010;51:899-908.
4. Morrell MJ; RNS System in Epilepsy Study Group. Responsive cortical stimulation for the treatment of medically intractable partial epilepsy. Neurology. 2011;77:1295-304.
5. Miranda MJ, Turner Z, Magrath G. Alternative diets to the classical ketogenic diet-Can we be more liberal? Epilepsy Res. 2012;100:278-85.
6. Neal EG, Chaffe H, Schwartz RH, Lawson MS, Edwards N, Fitzsimmons G, et al. The ketogenic diet for the treatment of childhood epilepsy: a randomised controlled trial. Lancet Neurol. 2008;7:500-6.
7. Cross JH, Neal EG. The ketogenic diet. Update on recent clinical trials. Epilepsia. 2008;49:6-10.