Definiciones
Epilepsia farmacorresistente o refractaria
La ILAE(1) propone en el año 2009 que la epilepsia farmacorresistente se debe definir como aquélla en la que se ha producido el fallo de tratamiento con dos terapias (bien en monoterapia o en combinación) correctamente indicadas y adecuadamente toleradas para alcanzar una remisión mantenida.
Epilepsia controlada
Cuando no ha habido crisis durante al menos tres veces el periodo de tiempo más largo que ha estado sin crisis en el último año antes de la nueva intervención o durante 12 meses (cualquiera de los criterios que sea más prolongado).
Ejemplos de definiciones
Un paciente que tiene una crisis cada 6 meses tendría que permanecer al menos 18 meses sin crisis para considerar que está respondiendo al nuevo tratamiento. En el otro extremo, un paciente que tiene una crisis al mes, debería estar al menos 12 meses sin crisis para considerar que ha respondido a la nueva intervención. En cualquiera de los dos casos, si existe recurrencia de crisis durante estos intervalos de tiempo se consideraría entonces como fallo del tratamiento. Dentro de esta nueva definición habrá un grupo de pacientes en los que todavía no sea posible realizar una clasificación en base al criterio temporal o de frecuencia de crisis (no han pasado todavía los 12 meses o 18 meses sin crisis si seguimos el ejemplo anterior) o en base al número de FAE probados (no han probado dos FAE en monoterapia o combinados). En estas situaciones, la ILAE, de acuerdo a la nueva definición, propone los términos "indefinido" e "indeterminado" respectivamente para clasificarlos temporalmente a la espera de que cumplan o no los criterios especificados anteriormente.
Indicaciones de cirugía de epilepsia
De forma general, se debe considerar cirugía de epilepsia en todo paciente con el diagnóstico de epilepsia focal con crisis no controladas pese a un tratamiento adecuado.
Requisitos
- • El paciente o la familia de éste, si no está capacitado, deben entender el objetivo de la cirugía, ya sea curativa o paliativa.
- • El paciente debe sufrir una epilepsia refractaria lo suficientemente grave como para valorar la opción quirúrgica.
- • No ha existido respuesta ni es esperable que exista a los distintos fármacos antiepilépticos disponibles.
- • La evaluación prequirúrgica ha permitido identificar un síndrome quirúrgico donde la cirugía puede ser eficaz.
- • El beneficio de la cirugía es muy superior al riesgo inherente al procedimiento quirúrgico y al asociado con seguir teniendo crisis.
- • No existe una enfermedad sistémica que contraindique la cirugía.
- • En caso de enfermedad psiquiátrica grave, ésta debe estar controlada.
Tipos
En función del objetivo de la cirugía se diferencia entre cirugía con intención curativa (control completo de las crisis) o cirugía paliativa (es probable que el paciente siga con crisis pero existe una posibilidad alta de que disminuyan las crisis en frecuencia e intensidad).
Definición de zona epileptógena
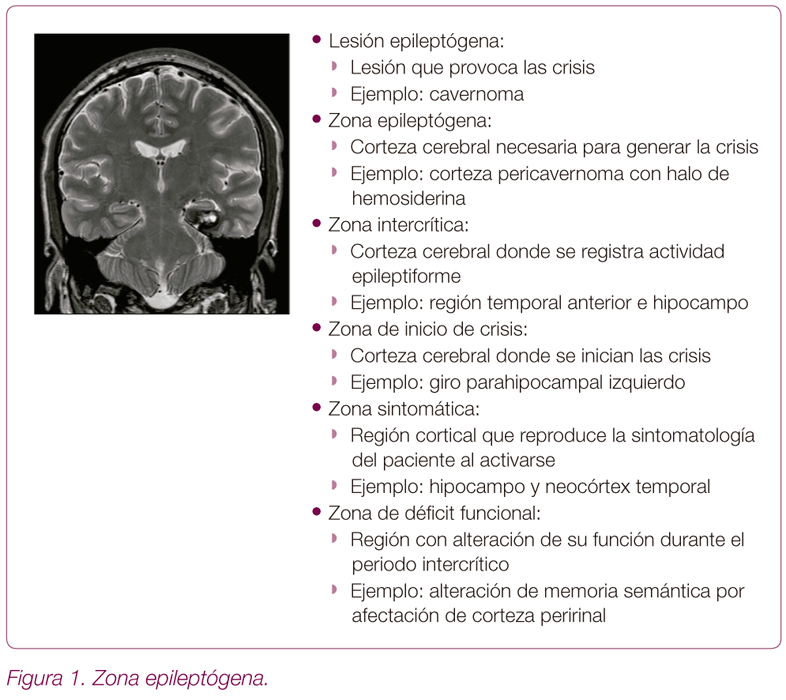
La Figura 1 representa de forma esquemática las distintas zonas que podemos delimitar en la evaluación prequirúrgica con la anamnesis, la exploración, la evaluación neuropsicológica y las diferentes pruebas de neuroimagen. Poder diferenciar estas zonas es importante de cara a una posible cirugía permitiendo realizar resecciones más dirigidas. En esta ilustración se muestra un cavernoma que afecta a giro parahipocampal izquierdo. En el caso presentado el paciente tendría unas posibilidades altas de quedarse sin crisis con la resección del cavernoma y el halo de hemosiderina que lo rodea. Pese a que la lesión se encuentra en proximidad del hipocampo y existe actividad epileptiforme sobre lóbulo temporal izquierdo es preferible conservar esta estructura por existir un elevado riesgo de pérdida de memoria y porque no participa en el inicio de las crisis en este paciente.
Evaluación prequirúrgica
Fase I
Estudio VEEG prolongado
- • Diagnóstico del tipo de epilepsia y tipo de crisis.
- • Análisis de la severidad de la epilepsia.
- • Aproximación a la zona epileptógena.
- ◗ Evaluación de la semiología de las crisis.
- ◗ Evaluación del EEG ictal/interictal.
Estudio neuropsicológico
- • Aproximación a la zona epileptógena.
- • Evaluación del riesgo quirúrgico.
- • Evaluación de comorbilidad psiquiátrica y funcionalidad.
Neuroimagen
- • RM cerebral (protocolo de epilepsia):
- ◗ Presencia de lesión que justifique la epilepsia.
- ◗ Planificación quirúrgica.
- ◗ Estudio de lenguaje y función motora/sensitiva.
- • Neuroimagen funcional (PET/SPECT/MEG) para localización de zona epileptógena si:
- ◗ RM cerebral negativa.
- ◗ Lesión no definitiva.
Fase II
Estudio con electrodos intracraneales
- • Localización de zona epileptógena.
- • Mapeo de funciones cerebrales.
- • Indicado en:
- ◗ RM cerebral negativa o no definitiva.
- ◗ Discordancia en la información obtenida en la fase I.
- ◗ Estudio de funciones cerebrales.
Test de WADA
- • Lateralización del lenguaje.
- • Estudio de memoria (riesgo de déficit severo de memoria).
- • Indicado en:
- ◗ Cirugía temporal hemisferio dominante.
- ◗ Sospecha de patología temporal bilateral.
- ◗ RM cerebral con hipocampos normales.
- ◗ Estudio neuropsicológico basal normal.
Algoritmo de evaluación prequirúrgica y tratamiento quirúrgico
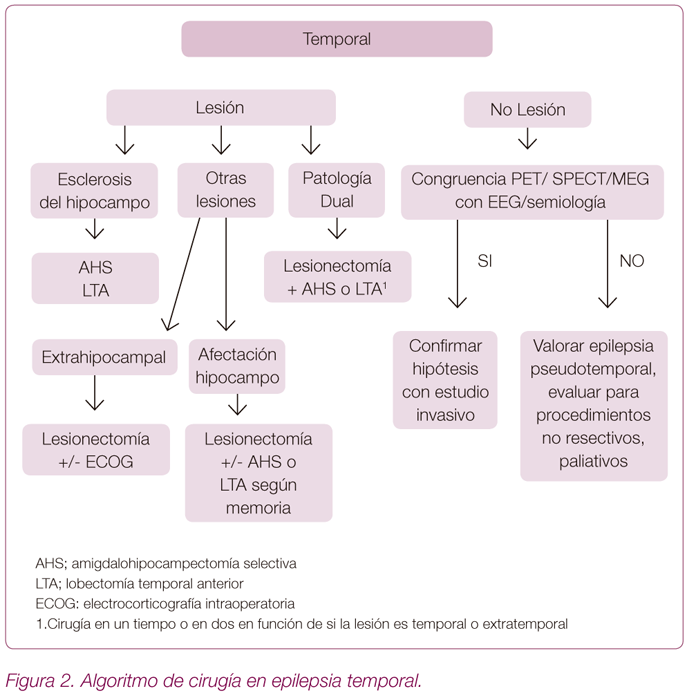
Epilepsia temporal (Figura 2)
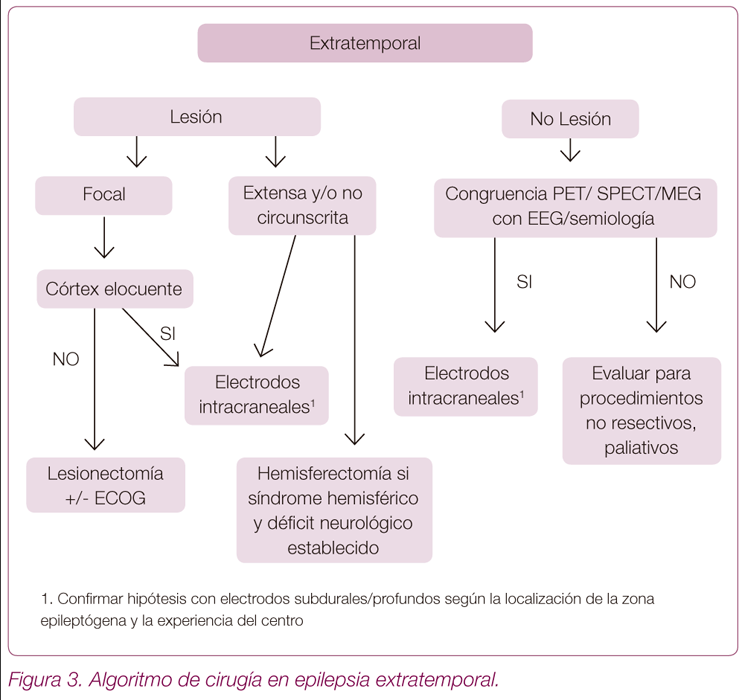
Epilepsia extratemporal (Figura 3)
Técnicas quirúrgicas (Tabla I)
Tabla I. Técnicas quirúrgicas.
Tipo de cirugía |
Descripción |
Indicación |
Lesionectomía +/- corticosectomía |
Resección de la lesión causante de la epilepsia +/- la corteza adyacente |
Cavernomas + anillo de hemosiderina Tumores gliales Astrocitomas de bajo grado |
Amígdalo-hipocampectomía |
Resección de amígdala e hipocampo |
Esclerosis medial. Mejores resultados si se reseca también giro parahipocampal. Posible menor déficit de memoria que en lobectomía temporal anterior sobre hemisferio dominante |
Lobectomía temporal anterior |
Resección de estructuras temporales mediales y neocorteza |
Esclerosis medial y lesiones temporales con afectación de hipocampo. En hemisferio dominante el margen posterior suele estar a 3 cm del polo temporal |
Lobectomía |
Resección anatómica de un lóbulo cerebral |
Lesiones extensas o no circunscritas como quistes porencefálicos, displasias o lesiones traumáticas |
Callosotomía |
Desconexión de ambos hemisferios a través de una incisión longitudinal sobre el cuerpo calloso |
Pacientes con síndrome de Lenox-Gastaut y otras epilepsias generalizadas sintomáticas. Especialmente indicado en crisis generalizadas tónico-clónicas o si las crisis cursan con caídas (drops-attacks). Puede ser limitada al tercio anterior del cuerpo calloso o total en pacientes con retraso intelectual severo |
Resecciones hemisféricas: Hemisferectomía anatómica Hemisferectomia funcional Hemisferotomía Hemicorticosectomía |
Resecciones que desconectan ambos hemisferios cerebrales: Hemisferectomía anatómica: resección del hemisferio cerebral Hemisferectomía funcional: desconexión hemisférica sin resección del parénquima Hemisferotomía perisilviana: desconexión hemisférica más resección de corteza perisilviana Hemicorticosectomía: resección de la corteza cerebral sin resección subcortical |
Síndromes hemisféricos: hemimegalencefalia, Sturge-Weber, S. Rasmussen, polimicrogiria, displasias extensas, porencefalia |
Transecciones subpiales múltiples |
Desconexión tangencial de la sustancia gris cortical sin interrumpir las proyecciones verticales a distancia |
Epilepsias focales con origen en corteza elocuente. Tiene el objetivo de preservar la función motora/sensitiva y el lenguaje. Los resultados son controvertidos |
Síndromes tratables quirúrgicamente
Definición
Epilepsia caracterizada por crisis frecuentes e invalidantes con una probabilidad baja de que se controlen/mejoren con fármacos antiepilépticos. Los síndromes tratables quirúrgicamente se caracterizan por:
- • Zona epileptógena identificada correctamente en la evaluación prequirúrgica.
- • Historia natural conocida siendo previsible que no exista una respuesta a futuros cambios de medicación.
- • La cirugía tiene una alta probabilidad de ayudar al paciente sin producir déficit neurológico invalidante.
En este sentido, cuando se identifica un síndrome epiléptico tratable quirúrgicamente no se debe demorar la cirugía durante años, sino hacer un uso razonable de los FAEs más apropiados para confirmar la refractariedad. Estudios recientes(3) indican que tras el fallo de seis FAEs correctamente seleccionados, las posibilidad de que exista respuesta a nuevos intentos terapéuticos es prácticamente nula.
Epidemiología
En todo paciente con epilepsia focal farmacorresistente se ha de realizar una evaluación prequirúrgica para determinar si es candidato a cirugía. La aplicación de estas técnicas permite identificar como potenciales candidatos quirúrgicos entre un cuarto y un tercio de los pacientes evaluados, aproximadamente un 5-10% de todos los pacientes con epilepsia refractaria. La mayoría de los paciente tratados quirúrgicamente sufren una epilepsia temporal lesional, no obstante las resecciones extratemporales pueden llegar a representar hasta un 30-40% de las intervenciones en cirugía de epilepsia, siendo las resecciones frontales las más frecuentes. La cirugía de epilepsia en los pacientes que son correctamente seleccionados controla o mejora la epilepsia en un 60-80% de los casos, proporciona una mayor calidad de vida y disminuye el coste médico a largo plazo.
Tipos de síndromes quirúrgicos
Síndromes lesionales focales
Esclerosis del hipocampo
- • Anatomía patológica (Tabla II)(4).
Tabla II. Anatomía patológica en la esclerosis del hipocampo.
|
Tipo Ia (Clásica) |
Tipo Ib (Severa) |
Tipo II (Esclerosis CA1) |
Tipo III (endofolio) |
Formas típicas |
Formas atípicas |
|||
Sectores del hipocampo con pérdida neuronal |
Pérdida neuronal severa en CA1 y moderada en los otros sectores |
Pérdida neuronal severa de todos los sectores |
Pérdida neuronal severa en CA1 y leve de otros sectores |
Pérdida neuronal severa en CA4 y leve de otros sectores |
En la Tipo Ia el subiculum y CA2 están preservados en comparación con CA1-CA4 que están más afectados. La mayor afectación de CA2 diferencia la tipo Ib de la Ia. Palimini et al, Neurology 2004
|
||||
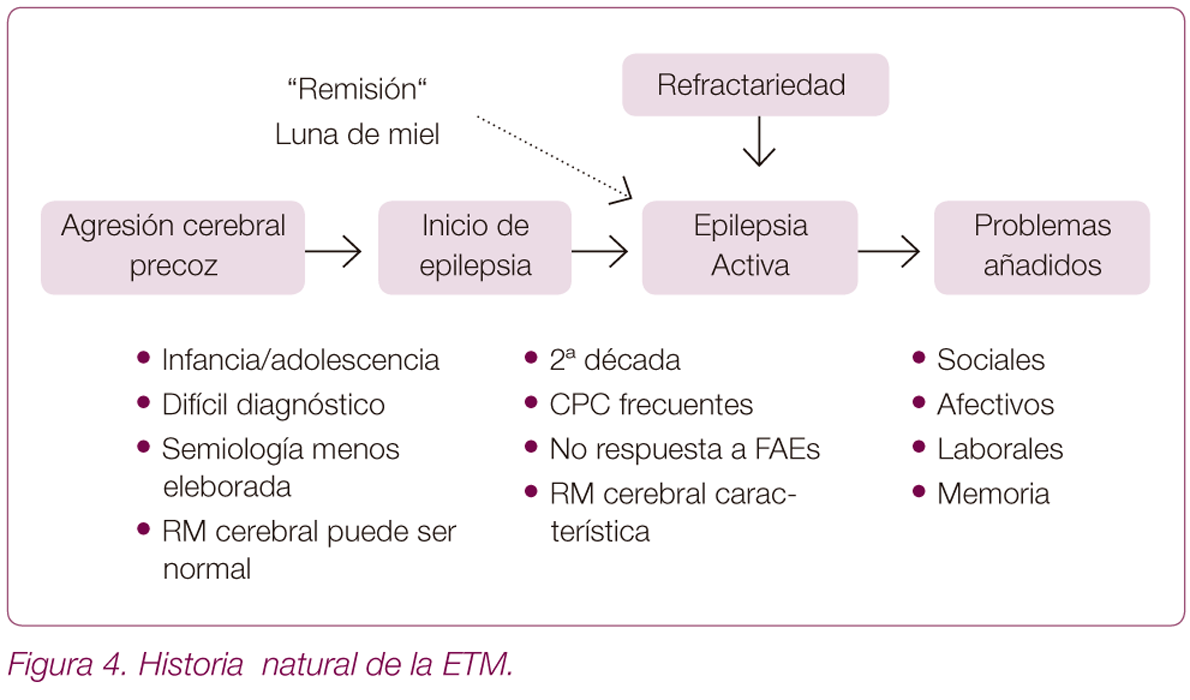
- • Características clínicas: la epilepsia temporal medial (ETM) asociada a la esclerosis del hipocampo (EH) representa hasta el 60-70% de las series quirúrgicas en pacientes adultos, siendo la epilepsia focal más frecuente. La historia natural de esta enfermedad es bastante característica (Figura 4): hasta 1/4-1/3 de los pacientes tienen antecedentes de crisis febriles, a continuación suele existir un periodo asintomático de varios años hasta la aparición de crisis espontáneas. La epilepsia suele aparecer en la primera década de la vida con crisis infrecuentes y de fácil control, conociéndose este periodo como "luna de miel". A partir de la segunda década la mayoría de los pacientes desarrollan una epilepsia farmacorresistente que cursa con crisis parciales simples y complejas y con un EEG característico (actividad theta temporal anterior izquierda con patrón evolutivo).
- • Características radiológicas: la RM cerebral muestra atrofia del hipocampo enfermo con disminución del volumen en secuencias T1 y T2 junto con aumento de señal en secuencias FLAIR y T2. De igual forma, se pueden observar otros signos indirectos como disminución del tamaño del lóbulo temporal ipsilateral, aumento del asta ventricular y cambios radiológicos a distancia (p. ej.: atrofia del fornix o del tálamo ipsilateral).
- • Resultados quirúrgicos: la mayoría de los pacientes son farmacorresistentes, con respuesta a los fármacos inferior a tasas al 20% en la mayoría de los estudios. La cirugía está indicada si no observa respuesta en los primeros años de tratamiento farmacológico. Se puede realizar una amígdalo-hipocampectomía selectiva o una lobectomía temporal anterior. Con cualquiera de las dos técnicas se obtienen buenos resultados con hasta un 80% de pacientes libres de crisis a largo plazo. Desde el punto de vista neuropsicológico hay estudios que muestran menor déficit de memoria con la amígdalo-hipocampectomía selectiva. En ambas técnicas los resultados son mejores si la resección incluye también el polo temporal y la corteza entorrinal (giro parahipocampal).
Patología dual
El concepto de patología dual hace referencia a pacientes con epilepsia focal con un estudio de neuroimagen que muestra una EH y otra lesión extrahipocampal potencialmente epileptógena. En la mayoría de los pacientes la lesión se encuentra en lóbulo temporal ipsilateral, no obstante la segunda lesión puede ser extratemporal. En algunas series quirúrgicas hasta un 15-30% de pacientes con epilepsia temporal refractaria presentan patología dual. Las crisis en estos pacientes se pueden originar en cualquiera de las dos lesiones. Los mejores resultados quirúrgicos se obtienen cuando ambas lesiones son resecadas completamente, con resultados similares a la cirugía de la ETM. De acuerdo a la localización de la segunda lesión, especialmente cuando ésta es extratemporal, se puede plantear una cirugía en dos tiempos.
Epilepsia bitemporal
El término epilepsia temporal bilateral o bitemporal hace referencia a epilepsias focales en las que se objetivan crisis epilépticas que se originan de forma independiente en cualquiera de los dos lóbulos temporales, generalmente procedentes de estructuras mediales. Con frecuencia pacientes con epilepsia temporal muestran datos de bilateralidad en las distintas pruebas de imagen (p. ej. atrofia hipocampal bitateral o hipometabolismo medial bilateral en el PET) o en el estudio neurofisiológico (hasta un tercio de pacientes con epilepsia temporal tienen puntas temporales bilaterales). Es importante recalcar que la bilateralidad en este grupo de pacientes es con frecuencia asimétrica y que la mayoría de las crisis proceden de una única zona epileptógena. La cirugía está especialmente indicada en pacientes con crisis unilaterales documentadas en el video-EEG con datos congruentes en otras pruebas (p. ej. que la RM cerebral y/o las pruebas de neuroimagen funcional y la evaluación neuropsicológica indiquen la afectación del mismo lado). En la mayoría de los pacientes está indicada monitorización invasiva con electrodos profundos o subdurales con el objetivo de identificar el lóbulo más activo.
Epilepsia vascular
La cirugía de epilepsia puede llegar a estar especialmente indicada en pacientes con cavernomas y malformaciones arteriovenosas. En los cavernomas, las crisis epilépticas son la presentación clínica más frecuente y el riesgo de desarrollar epilepsia es del 4-11% al año. En las malformaciones arteriovenosas, el riesgo de epilepsia es inferior al de los cavernomas, con un riesgo aproximado de 1% al año. La indicación de tratamiento quirúrgico debe considerarse en: 1) pacientes con crisis refractarias y lesión abordable quirúrgicamente, 2) pacientes con hemorragia cerebral y crisis, con independencia de que las crisis estén controladas o no. En esta segunda situación clínica el objetivo principal de la cirugía es disminuir el riesgo de resangrado. Los mejores resultados quirúrgicos se obtienen cuando además de resecar la lesión se elimina el córtex adyacente y el halo de hemosiderina perilesional. Los resultados quirúrgicos son positivos con un 70-80% libre de crisis.
Epilepsia tumoral
Las crisis epilépticas son el síntoma de presentación más frecuente de los tumores cerebrales de bajo grado celular y con lento crecimiento. Hasta el 50% de los pacientes con tumores cerebrales presentan alguna crisis en el transcurso de su enfermedad. Los tumores de menor grado y con localización temporal pueden tener mayor riesgo de desarrollar epilepsia con respecto a otras localizaciones (Tabla III). Entre un 12-50% de los pacientes desarrollarán una epilepsia refractaria. El abordaje quirúrgico en pacientes con epilepsia refractaria por tumores cerebrales depende del tipo de tumor, de la localización y de la extensión del mismo; en pacientes con tumores de alto grado con un pronóstico vital disminuido el objetivo de la cirugía es reducir la masa tumoral lo máximo posible y obtener un muestra histológica que confirme el diagnóstico y ayude a planificar el tratamiento más adecuado. En el contexto clínico diferente de tumores de bajo grado y epilepsia (p. ej. astrocitomas, oligodendrogliomas gangliomas o DNET), el objetivo de la cirugía no sólo debe ser el de la extirpación del tumor sino además el control de la crisis. Los resultados quirúrgicos en estos pacientes son positivos con hasta un 80% libre de crisis en algunas series. Son factores de buen pronóstico la resección total del tumor, cuando se tratan de tumores con bajo poder proliferativo y en algunos trabajos la intervención precoz.
Tabla III. Tipo de tumor y riesgo de epilepsia.
Tipo de tumor |
Riesgo de epilepsia |
Tumor neuroepitelial disembrioplásico |
>90% |
Ganglioglioma |
80-90% |
Oligodendroglioma |
70-80% |
Astrocitoma de bajo grado |
70-80% |
Meningioma |
20-60% |
Astrocitoma de alto grado |
30-50% |
Linfoma primario |
10% |
Síndromes lesionales no circunscritos y/o extensos
Epilepsia temporal no lesional
La epilepsia temporal no lesional se puede dividir en dos grupos: la que se origina en neocórtex y la que se origina en estructuras mediales. Aún encontrándonos con pacientes con RM cerebral negativa, el análisis semiológico puede indicar si las crisis se originan en estructuras mediales o en corteza lateral (Tabla IV). En estos pacientes la evaluación prequirúrgica debe incluir estudios de neuroimagen funcional (PET y/o SPECT/SISCOM) que junto con la semiología y los hallazgos del VEEG nos pueden ayudar a localizar mejor la zona epileptógena. Cuando los resultados de estas pruebas son congruentes entre sí los resultados quirúrgicos pueden ser satisfactorios con hasta un 60-70% de pacientes libres de crisis. No obstante, algunos autores recomiendan realizar un estudio invasivo con electrodos intracraneales en este grupo de epilepsias para confirmar que efectivamente el origen de las crisis es temporal; existe la posibilidad de que estas pruebas sean falsamente localizadoras y que las crisis se originen en regiones extratemporales y propaguen a lóbulo temporal. De igual forma, el estudio invasivo puede diferenciar si las crisis se originan en hipocampo vs neocórtex, permitiendo ser más selectivo en la cirugía.
Tabla IV. Diferencias clínicas entre epilepsia temporal medial y neocortical.
Manifestaciones |
Epilepsia temporal medial |
Epilepsia temporal neocortical |
Crisis febril |
Sí |
No |
Tipo de aura |
Epigástrica |
Visual/auditiva |
Aura Psíquica |
Frecuente |
Infrecuente |
Automatismos orales |
Frecuentes (más precoces) |
Escasos y tardíos |
"Desconexión" Reacción de parada |
Tardía |
Precoz |
Duración |
Más prolongadas |
Breves |
Crisis generalizadas |
Infrecuente |
Frecuente |
Distonía ES |
Tardía |
Precoz |
Epilepsia pseudotemporal o temporal plus
El término epilepsia pseudotemporal o temporal plus hace referencia a un grupo de pacientes con epilepsia focal sin lesión en la RM cerebral que presentan crisis con semiología temporal, con hallazgos electroencefalográficos y/o de neuroimagen que también pueden apoyar erróneamente un origen temporal, cuando realmente la zona epileptógena es extratemporal. En estos pacientes, si se valora cirugía de la epilepsia, siempre hay que realizar previamente una evaluación invasiva con electrodos intracraneales. Semiológicamente existen manifestaciones y/o signos que nos pueden hacer pensar que estamos ante un paciente con epilepsia pseudotemporal (Tabla V).
Tabla V. Diferencias clínicas entre epilepsia temporal y pseudotemporal.
Manifestaciones |
Epilepsia temporal |
Epilepsia Pseudotemporal |
Tipo de aura |
Epigástrica |
Auditiva, vestibular, gustativa |
Automatismos |
Gestuales |
Manifestaciones motoras simples |
Alteración de consciencia |
Tardía |
Precoz |
Periodo postictal |
Amnesia postictal |
Disforia postictal |
Actividad epileptiforme |
Temporal |
Extratemporal |
Epilepsia extratemporal no lesional
Representan el grupo de epilepsias donde el abordaje quirúrgico es más complicado. De entre las distintas localizaciones, en las series quirúrgicas predominan las cirugías frontales. A diferencia de otros síndromes quirúrgicos, los resultados en este grupo de pacientes son inferiores (generalmente <50-60% libre de crisis). Las razones que justifican peores resultados se deben a: 1) zona epileptógena extensa o multifocal, 2) las pruebas de neuroimagen funcional pueden tener un menor rendimiento diagnóstico, 3) el electroencefalograma puede ser falsamente localizador, 4) la zona epileptégena puede coincidir o estar adyacente con una zona elocuente. Por las razones anteriores en todos los pacientes se debe realizar una evaluación con electrodos intracraneales (subdurales y/o profundos). Los resultados quirúrgicos son más favorables en aquellos pacientes donde el estudio con electrodos intracraneales muestre patrones focales congruentes con los hallazgos de la evaluación prequirúrgica. No obstante, debido a la dificultad diagnóstica en estos pacientes, hasta en un 20-40% de las evaluaciones invasivas los electrodos se retiran sin llegar a identificar la localización de la zona epileptogéna.
Displasia cortical focal
- • Anatomía patológica: la displasia cortical focal (DCF) en un subtipo de malformación del desarrollo cortical (MDC) en la que la afectación cerebral es en su mayoría intracortical. La nueva clasificación de la ILAE(5) diferencia varios tipos en función del grado de alteración cortical (Tabla VI). Desde el punto de vista histológico la DCF tipo II es más severa que la tipo I. La principal diferencia entre ambos subtipos es la presencia de neuronas dismórficas-citomegálicas y células globoides. En la nueva clasificación, la DFC tipo III hace referencia a DFC asociadas a otro tipo de lesiones.
Tabla VI. Clasificación anatomopatológica de las displasias corticales focales (DCF).
DCF tipo I |
Tipo IA |
Tipo IB |
Tipo IC |
||||
Alteración de la laminación cortical radial |
Alteración de la laminación cortical tangencial |
Alteración de la laminación cortical radial y tangencial |
|||||
DCF tipo II |
Tipo IIA |
Tipo IIB |
|||||
Alteración severa de la laminación cortical + neuronas dismórficas |
Alteración severa de la laminación cortical + neuronas dismórficas y células balonadas |
||||||
DCF tipo III (Asociada a otra lesión) |
Tipo IIIA |
Tipo IIIB |
Tipo IIIC |
Tipo IIID |
|||
Alteración de la laminación cortical temporal + esclerosis del hipocampo |
Alteración de la laminación cortical adyacente a tumor neuroglial |
Alteración de la laminación cortical adyacente a malformación vascular |
Alteración de la laminación cortical adyacente a lesión precoz |
||||
- • Características clínicas: la DFC representa la indicación quirúrgica más frecuente en pacientes menores de 18 años y la tercera en adultos de acuerdo a algunos registros. Las DFC tipo II se asocian a una epilepsia más severa que se caracteriza por empezar a edades más tempranas y crisis más graves. Este tipo de lesión suele ser más extensa, de localización extratemporal, otras veces hemisférica o multilobar.
- • Características radiológicas: la RM cerebral estructural es muy característica cuando es positiva aunque no permite establecer el grado histológico de una forma definitiva en la mayoría de los casos. La DFC tipo I suele ser más circunscrita en la RM cerebral y afecta más frecuentemente el lóbulo temporal. No obstante, sólo la presencia de alteración de la señal de la sustancia blanca con comunicación entre el ventrículo y la corteza (transmantle displasia) permite diferenciar la DFC tipo II de la tipo I. La RM cerebral, especialmente en la tipo I, puede ser negativa hasta en un 40% de los casos. Además, en las displasias más severas la alteración histológica suele ser más extensa que la mostrada por la neuroimagen. Por ello en la mayoría de los pacientes la evaluación prequirúrgica suele incluir pruebas de neuroimagen funcional (PET y/o SISCOM) y finalmente la implantación de electrodos intracraneales para delimitar mejor la zona epileptógena.
- • Resultados quirúrgicos: la cirugía en estos pacientes puede estar indicada tan pronto como se confirme farmacorresistencia. El factor pronóstico más importante en la cirugía de la DFC es la resección completa del tejido displásico. Los resultados quirúrgicos varían entre las distintas series con una tasa del 60-80% de pacientes intervenidos libres de crisis cuando la resección es completa. Son factores de mal pronóstico las displasias extensas, la localización fuera del lóbulo temporal y la ausencia de un patrón EEG localizador. Existe controversia entre el grado histológico y los resultados quirúrgicos.
Polimicrogiria y esquisencefalia
La polimicrogiria es una de la MDC más frecuentes que se asocian a epilepsia, caracterizada por una alteración de la laminación y del patrón giral de la corteza cerebral. La esquisencefalia es una MDC caracterizada por una hendidura en el espesor de la corteza cerebral en dirección al ventrículo, cubierta por corteza polimicrogírica. Ambos tipos de lesiones suelen localizarse con más frecuencia en la corteza perisilviana, con frecuencia bilateralmente, no obstante se describen en otras localizaciones. El origen de este tipo de MDC puede ser multifactorial, en la actualidad se clasifican dentro de las alteraciones que aparecen en las fases tardías de la migración neuronal o en las primeras fases de la organización cortical. El candidato quirúrgico más frecuente en este tipo de MCD es el paciente con una epilepsia focal y un déficit neurológico establecido por la propia lesión donde la RM cerebral muestra una afectación unilateral.
Heterotopia nodular
MCD caracterizada por la agrupación nodular de neuronas revistiendo las paredes de los ventrículos o a nivel subcortical, con distribución uni- o bilateral, con frecuencia asociada a otras MCD. Se han publicado resultados positivos en pacientes con heterotopias subcorticales y periventriculares unilaterales donde la resección incluye la heterotopia y la corteza displásica adyacente con la que está relacionada.
Hemimegalencefalia
MCD severa caracterizada por el sobrecrecimiento y alteración de la estructura de un hemisferio cerebral. A nivel patológico existe una alteración de la laminación cortical y de la sustancia blanca subcortical, con alteración de los giros corticales que aparecen engrosados y aumento del sistema ventricular en el hemisferio afectado. La evolución natural en esta enfermedad se caracteriza por una epilepsia severa con inicio en los primeros meses o años de vida, retraso psicomotor y hemiparesia/hemianopsia que pueden aparecer desde el debut de la epilepsia o en el transcurso de la enfermedad. En otras ocasiones se puede presentar formando parte de diferentes facomatosis. La cirugía en este síndrome quirúrgico tiene el objetivo de desconectar al hemisferio enfermo del sano, empleándose diferentes técnicas hemisféricas (p. ej., hemisferectomías o hemicorticetomía) con resultados positivos en hasta un 50% de los pacientes.
Hamartoma hipotalámico
Los hamartomas hipotalámicos (HH) son malformaciones congénitas no neoplásicas que se localizan en el hipotálamo, entre el tallo infundibular y los cuerpos mamilares. La epilepsia en estos pacientes aparece en los primeros años de vida y se caracteriza por: a) crisis de risa inmotivada (crisis gelásticas) y a veces de lloro (crisis dacrísticas) en el debut de la enfermedad, siendo las crisis más frecuentes que caracterizan la enfermedad, b) encefalopatía epiléptica con deterioro cognitivo progresivo y distintos tipos de crisis en las formas más severas, c) pubertad precoz en algunos pacientes, d) síndrome de Pallister-Hall en formas hereditarias. El tratamiento farmacológico suele ser ineficaz en el control de las crisis. Aunque no está estandarizado, la radiocirugía esterotáxica es especialmente eficaz en HH pequeños intrahipotalámicos o en proximidad con el III ventrículo, con respuesta clínica en un 60% de los pacientes tratados a partir de 1-2 años del tratamiento. La cirugía convencional puede estar más indicada en los HH de mayor tamaño, tratamiento que se puede completar con radiocirugía. En algunos centros se utiliza la braquiterapia con resultados también positivos.
Encefalitis de Rassmusen
La cirugía (hemisferectomía anatómica, hemisferotomía o hemicorticectomía) está indicada especialmente en aquellos casos que no responden a tratamiento farmacológico y presentan un déficit neurológico establecido, especialmente una hemiparesia, controlando las crisis en un 60-80% de los pacientes intervenidos.
Síndrome de Sturge-Weber
La cirugía de la epilepsia está indicada en las formas más severas, realizándose resecciones parciales en las formas más circunscritas y hemisferectomías en las formas hemisféricas o más extensas.
Esclerosis tuberosa
El candidato quirúrgico ideal es aquel en el que la RM cerebral muestra un único túber con localización en áreas no elocuentes y existe una correlación electroclínica evidente. En estas circunstancias los resultados quirúrgicos son muy positivos con alrededor de un 80% de pacientes libres de crisis. Cuando existen varios túberes los resultados son inferiores. Además, la epileptogenicidad de los túberes puede modificarse a lo largo de la enfermedad y pasar de un túber a otro. Pese a estas dificultades la cirugía de epilepsia puede ser una opción en un subgrupo de pacientes en los que consigamos demostrar el túber o los túberes responsables de las crisis. En este grupo de pacientes la evaluación prequirúrgica debe ser más extensa e incluir pruebas de neuroimagen funcional y exploración con electrodos intracraneales.
Encefalomalacia y porencefalia
La encefalomalacia y porencefalia son lesiones cerebrales destructivas que pueden tener un origen isquémico, traumático o infeccioso. Ambos tipos de lesiones se asocian con frecuencia a una epilepsia que puede ser farmacorresistente en muchos casos. Las lesiones porencefálicas son frecuentes en niños que han sufrido un infarto perinatal y pueden evolucionar a síndromes hemisféricos con hemiplejia. Los resultados quirúrgicos son buenos cuando existe un claro correlato electro-clínico y las lesiones son unilaterales, siendo generalmente pacientes subsidiarios de hemisferectomías. Los resultados quirúrgicos también son positivos en pacientes con ulegiria; se trata de una encefalopatía hipóxico-isquémica en gestaciones a término, con afectación bilateral del territorio frontera entre ACM y ACP, de predominio posterior y que generalmente se asocia a epilepsia occipital.
Factores pronósticos en cirugía de epilepsia
- • RM cerebral: identificación de una lesión epileptógena vs RM negativa.
- • Tipo de lesión: mejores resultados en lesiones circunscritas como tumores de bajo grado en comparación con lesiones no circunscritas como malformaciones del desarrollo cortical donde la resección puede que no llegue a ser completa.
- • Histología: identificación de un sustrato patológico establecido en el estudio patológico vs patología negativa.
- • Localización: de forma general los resultados son mejores en cirugías temporales vs extratemporales en gran medida por la complejidad de la evaluación prequirúrgica en este último grupo.
- • Duración de epilepsia: en algunas estudios mejores resultados quirúrgicos si la cirugía no se demora muchos años, tras confirmar farmacorresistencia.
Factores pronóstico en epilepsia temporal (Tabla IV)
Tabla VII. Factores pronósticos en epilepsia temporal.
Clínicos |
Neurofisiológicos |
Neuroimagen |
Antecedentes de crisis febriles |
AEI unilateral >90% |
EH unilateral |
Epilepsia de corta duración |
AEI unilateral infrecuente (<60 puntas/horas ) |
Concordancia RM cerebral y EEG interictal |
Semiología característica Pocas crisis (<20/mes) |
Ausencia de AEI extratemporal, temporal posterior, bitemporal, generalizada |
Hipometabolismo unilateral en PET |
Ausencia de crisis SGTC |
Patrón ictal (theta) temporal anterior |
Hiperperfusión ictal unilateral en SPECT |
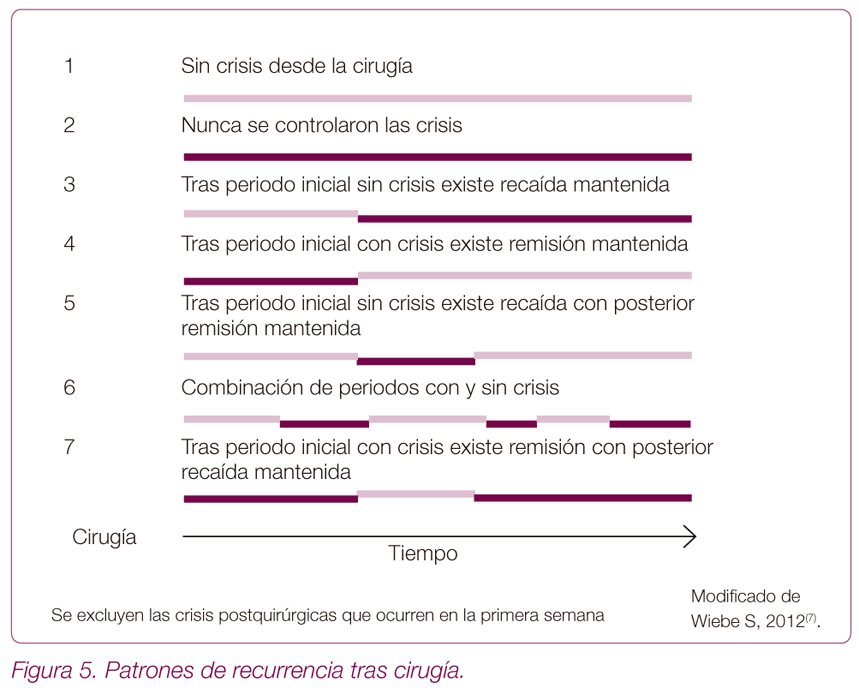
Patrones de recurrencia tras cirugía (Figura 5)
Medicación tras cirugía
Es controvertido como hay que manejar el tratamiento tras la cirugía en un paciente que finalmente se controla. En los diferentes estudios entre un 20-60% de pacientes permanecerán sin crisis al retirar la medicación(9,10). No obstante son escasos e incompletos los estudios que pueden responder a la pregunta de cómo y cuándo simplificar el tratamiento farmacológico en un paciente controlado tras cirugía de epilepsia. La tendencia habitual en algunos centros es esperar a 1-2 años sin crisis para iniciar la retirada de uno de los fármacos que el paciente esté tomando si recibe politerapia y progresivamente en los siguientes años ir reduciendo/suspendiendo los demás.
Factores de riesgo de recurrencia postquirúrgicos
- • RM cerebral negativa.
- • Estudio patológico negativo (no se identifica ninguna lesión).
- • Recurrencia tras la cirugía antes de iniciar la retirada de medicación.
- • Epilepsia de larga evolución antes de la cirugía.
- • Inicio precoz de retirada de medicación (<9 meses)(8).
- • Persistencia de actividad epileptiforme en los EEGs de control postquirúrgicos.
Clasificaciones en cirugía de epilepsia
Clasificación postquirúrgica de la ILAE (Tabla VII)
Tabla VIII. Clasificación postquirúrgica de la ILAE.
Clasificación |
Resultados |
1 |
No crisis ni auras |
2 |
Sólo auras |
3 |
1-3 días con crisis al año +/- auras |
4 |
De 4 días con crisis al año a una reducción del 50% de los días con crisis +/- auras |
5 |
De menos de una reducción del 50% de los días con crisis a un aumento del 100% de los días con crisis +/- auras |
6 |
Aumento de más de un 100% de los días con crisis +/- auras |
En los apartados 4-6 la reducción o aumento de los días con crisis se deben comparar con la situación basal previa a la cirugía que corresponde al número de días con crisis durante los 12 meses antes de la cirugía.
Modificado de Wieser HG et al, 2001(9).
Clasificación postquirúrgica de Engel (Tabla IX)
Tabla IX. Clasificación postquirúrgica de Engel (modificada).
Clasificación |
Definición |
Clase I Libre de crisis |
A: Sin crisis desde la cirugía a B: Tan sólo crisis parciales simples no incapacitantes desde la cirugía C: Algunas crisis incapacitantes después de la cirugía, pero al menos dos años sin crisis incapacitantes desde la cirugía D: Crisis con actividad convulsiva tan sólo al retirar la medicación |
Clase II Crisis incapacitantes infrecuentes |
A: Inicialmente sin crisis pero ahora tiene crisis infrecuentes B: Crisis infrecuentes desde la cirugía C: Crisis incapacitantes inicialmente, pero infrecuentes en los dos últimos años D: Tan sólo crisis nocturnas |
Clase III Mejoría significativa ("la cirugía merece la pena") |
A: Reducción significativa de crisis (>90% respecto a situación basal) B: Intervalos prolongados libres de crisis por un tiempo superior a la mitad del periodo de seguimiento pero no superior a dos años |
Clase IV No mejoría significativa ("la cirugía no merece la pena") |
A: Reducción significativa de crisis (entre 50-90%) B: No se aprecia mejoría (reducción < 50%) C: Empeoramiento de crisis |
Modificado de Engel et al, 1993(10). |
|
Bibliografía
1. Kwan P, Arzimanoglou A, Berg AT, Brodie MJ, Allen Hauser W, Mathern G, et al. Definition of drug resistant epilepsy: consensus proposal by the ad hoc Task Force of the ILAE Commission on Therapeutic Strategies. Epilepsia. 2010;51:1069-77.
2. Kwan P, Brodie MJ. Early identification of refractory epilepsy. N Engl J Med. 2000;342:314-9.
3. Schiller Y, Najjar Y. Quantifying the response to antiepileptic drugs. Effect of past treatment history. Neurology. 2008;70:54–65
4. Blümcke I, Pauli E, Clusmann H, Schramm J, Becker A, Elger C, et al. A new clinico-pathological classification system for mesial temporal sclerosis. Acta Neuropathol. 2007;113:235-44.
5. Blümcke I, Thom M, Aronica E, Armstrong DD, Vinters HV, Palmini A, et al. The clinicopathologic spectrum of focal cortical dysplasias: a consensus classification proposed by an ad hoc Task Force of the ILAE Diagnostic Methods Commission. Epilepsia. 2011;52:158-74.
6. Spencer S, Huh L. Outcomes of epilepsy surgery in adults and children. Lancet Neurol. 2008;7:525-37.
7. Wiebe S. Epilepsy. Outcome patterns in epilepsy surgery--the long-term view. Nat Rev Neurol. 2012;8:123-4.
8. Park KI, Lee SK, Chu K. Withdrawal of antiepileptic drugs after neocortical epilepsy surgery. Ann Neurol. 2010;67:230-8.
9. Wieser HG, Blume WT, Fish D. ILAE Commission Report. Proposal for a new classification of outcome with respect to epileptic seizures following epilepsy surgery. Epilepsia. 2001;42:282-6.
10. Engel J Jr, Van Ness P, Rasmussen TB, Ojemann LM. Outcome with respect to epileptic seizures. In: Engel J Jr, ed. Surgical treatment of the epilepsies. 2nd ed. New York: Raven Press; 1993. p. 609-21.
Tratamiento